Chất hoá học (NH2)2CO (ure)
Xem thông tin chi tiết về chất hoá học (NH2)2CO (ure)
Tìm kiếm chất hóa học
Hãy nhập vào chất hoá học để bắt đầu tìm kiếm
Giới thiệu
Chất hoá học (NH2)2CO (ure)
Urê là một hợp chất nitơ có chứa một nhóm cacbonyl gắn với hai nhóm amin có hoạt tính lợi tiểu thẩm thấu. Trong cơ thể sống, urê...
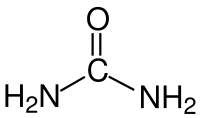
Thông tin chi tiết về chất hoá học (NH2)2CO
- Công thức tổng quát CH4N2O
- Tên quốc tế: đang cập nhật...
- Nguyên tử khối: 60.0553
- Màu sắc: 126
- Nhiệt độ sôi: đang cập nhật...
- Nhiệt độ nóng chảy: 133
- Trạng thái: 121
Ứng dụng của (NH2)2CO trong thực tế
Urê là một hợp chất nitơ có chứa một nhóm cacbonyl gắn với hai nhóm amin có hoạt tính lợi tiểu thẩm thấu. Trong cơ thể sống, urê được hình thành trong gan thông qua chu trình urê từ amoniac và là sản phẩm cuối cùng của quá trình chuyển hóa protein. Việc sử dụng urê làm tăng độ thẩm thấu huyết tương, dẫn đến tăng cường dòng chảy của nước từ các mô, bao gồm não, dịch não tủy và mắt, vào dịch kẽ và huyết tương, do đó làm giảm áp lực trong các mô đó và tăng lượng nước tiểu ra ngoài. Nó có vai trò như chất xử lý bột mì, chất chuyển hóa ở người, chất chuyển hóa Daphnia magna, chất chuyển hóa Saccharomyces cerevisiae, chất chuyển hóa Escherichia coli, chất chuyển hóa của chuột và phân bón. Nó là một amit axit monocacboxylic và một hợp chất một cacbon .
1. Ứng dụng
a. Sử dụng phân bón trong nông nghiệp
Hơn 90% sản lượng ure công nghiệp trên thế giới được sử dụng làm phân bón nhầm cung cấp nito cho cây trồng. Trong số các loại phân bón cung cấp đạm, thì ure là phân bón có hàm lượng nito cao nhất trong taatscar các loại phân bón.
Do đó, nó có chi phí vận chuyển thấp trên một đơn vị dinh dưỡng nitơ . Tạp chất phổ biến nhất của urê tổng hợp là biuret, làm giảm sự phát triển của thực vật. Urê phân hủy trong đất để tạo ra amoni. Amoni được thực vật hấp thụ. Trong một số loại đất, amoni bị ôxy hóa bởi vi khuẩn để tạo ra nitrat, đây cũng là một chất dinh dưỡng thực vật. Việc thất thoát các hợp chất nitơ vào khí quyển và nước chảy tràn vừa lãng phí vừa gây tổn hại đến môi trường. Vì lý do này, urê đôi khi được xử lý trước hoặc biến đổi để nâng cao hiệu quả sử dụng trong nông nghiệp. Một trong những công nghệ như vậy là phân bón giải phóng có kiểm soát , có chứa urê được bao bọc trong một chất trám trét trơ. Một công nghệ khác là chuyển đổi urê thành các dẫn xuất, chẳng hạn như với formaldehyde, phân hủy thành amoniac với tốc độ phù hợp với nhu cầu dinh dưỡng của cây trồng.
 Hơn 90% sản lượng ure công nghiệp trên thế giới được sử dụng làm phân bón nhầm cung cấp nito cho cây trồng. Trong số các loại phân bón cung cấp đạm, thì ure là phân bón có hàm lượng nito cao nhất trong taatscar các loại phân bón.
Hơn 90% sản lượng ure công nghiệp trên thế giới được sử dụng làm phân bón nhầm cung cấp nito cho cây trồng. Trong số các loại phân bón cung cấp đạm, thì ure là phân bón có hàm lượng nito cao nhất trong taatscar các loại phân bón.
b. Nhựa
Urê là nguyên liệu để sản xuất hai loại vật liệu chính: nhựa urê-formaldehyde và urê-melamine-formaldehyde được sử dụng trong ván ép hàng hải
c. Hệ thống ô tô
Urê được sử dụng trong Selective Non-Catalytic Reduction (SNCR) và Selective Catalytic Reduction (SCR) phản ứng để giảm NOx các chất ô nhiễm trong khí thải từ đốt từ dầu diesel , nhiên liệu kép, và nạc-đốt khí thiên nhiên động cơ. Các Bluetec hệ thống, ví dụ, tiêm dung dịch urê nước dựa vào hệ thống ống xả. Amoniac được tạo ra từ quá trình thủy phân urê phản ứng với khí thải nitơ oxit và được chuyển hóa thành nitơ và nước trong bộ chuyển đổi xúc tác. Xe tải và ô tô sử dụng các bộ chuyển đổi xúc tác này cần mang theo nguồn cung cấp dầu xả diesel , dung dịch urê trong nước.
d. Phòng thí nghiệm
Ure với nồng độ 10 M là một chất biến tính protein mạnh vì nó phá vỡ các liên kết không hóa trị trong protein. Tính chất này có thể được khai thác để tăng khả năng hòa tan của một số protein. Hỗn hợp ure và choline clorua được sử dụng làm dung môi eutectic sâu (DES), một chất tương tự như chất lỏng ion.
e. Sử dụng y tế
Các loại kem có chứa ure được sử dụng như các sản phẩm da liễu tại chỗ để thúc đẩy quá trình bù nước cho da. Ure 40% được chỉ định cho bệnh vẩy nến, xerosis, nấm móng, ichthyosis, eczema, dày sừng, keratoderma, ngô, vết chai.
Bên cạnh đó, các nhà khoa học đã nghiên cứu và thấy được rằng ure có tác dụng như một chất lợi tiểu và được sử dụng đầu tiên bởi Tiến Sĩ W.Friedrich vào năm 1892. Một nghiên cứu vào năm 2010 trên các bệnh nhân CIU, ure được sử dụng để điều trị bệnh hạ natri máu thể tích và được cho là an toàn, rẻ tiền và đơn giản.
Trước đây, ure đã được dùng vào mục đích phá thai. Ngoài ra, các ure máu nito (BUN) kiểm tra là thước đo lượng nito trong máu xuất phát từ ure.
Urea cũng đã được nghiên cứu như một tá dược trong công thức thuốc phủ Balloon (DCB) để tăng cường phân phối thuốc tại chỗ đến các mạch máu nhiễm mỡ. Urê, khi được sử dụng như một tá dược với liều lượng nhỏ (~ 3μg / mm 2 ) để phủ lên bề mặt DCB đã được tìm thấy để tạo thành các tinh thể làm tăng chuyển thuốc mà không có tác dụng độc hại lên tế bào nội mô mạch máu .
Urê có nhãn carbon-14 hoặc carbon-13 được sử dụng trong xét nghiệm urê hơi thở , được sử dụng để phát hiện sự hiện diện của vi khuẩn Helicobacter pylori ( H. pylori ) trong dạ dày và tá tràng của người, có liên quan đến loét dạ dày tá tràng . Thử nghiệm phát hiện enzyme urease đặc trưng , được tạo ra bởi H. pylori , bằng phản ứng tạo ra amoniac từ urê. Điều này làm tăng độ pH (giảm độ axit) của môi trường dạ dày xung quanh vi khuẩn. Các loài vi khuẩn tương tự với H. pylori có thể được xác định bằng xét nghiệm tương tự trên động vật như vượn, chó và mèo (kể cả mèo lớn ).
f. Một số ứng dụng khác
- Một thành phần trong chất lỏng xả động cơ diesel (DEF), là 32,5% urê và 67,5% nước khử ion. DEF được phun vào dòng khí thải của xe chạy bằng động cơ diesel để phân hủy lượng khí thải NOx nguy hiểm thành nitơ và nước vô hại.
- Một chất thay thế không ăn mòn cho muối mỏ để khử băng trên đường . Nó thường là thành phần chính của các chất thay thế muối thân thiện với vật nuôi mặc dù nó kém hiệu quả hơn so với muối mỏ truyền thống hoặc clorua canxi.
- Là một chất phụ gia tăng cường độ hòa tan và giữ ẩm cho các dung dịch nhuộm để nhuộm vải hoặc in.
2. Vai trò sinh học
Các axit amin từ thức ăn được sử dụng để tổng hợp protein và các chất sinh học khác - hoặc được tạo ra từ quá trình dị hóa protein cơ - được cơ thể oxy hóa như một nguồn năng lượng thay thế, tạo ra urê và carbon dioxide. Con đường oxy hóa bắt đầu bằng việc loại bỏ nhóm amin bởi một transaminase ; nhóm amin sau đó được đưa vào chu trình urê . Bước đầu tiên trong quá trình chuyển đổi axit amin từ protein thành chất thải trao đổi chất trong gan là loại bỏ nitơ alpha-amino, tạo ra amoniac. Vì amoniac là chất độc nên được cá bài tiết ngay lập tức, chuyển hóa thành axit uricbởi chim, và chuyển hóa thành urê của động vật có vú.
Amoniac (NH3 ) là một sản phẩm phụ phổ biến của quá trình chuyển hóa các hợp chất nitơ. Amoniac nhỏ hơn, dễ bay hơi hơn và di động hơn urê. Nếu được phép tích tụ, amoniac sẽ làm tăng độ pH trong tế bào lên mức độc hại. Do đó, nhiều sinh vật chuyển đổi amoniac thành urê, mặc dù sự tổng hợp này có chi phí năng lượng ròng. Thực tế là trung tính và hòa tan cao trong nước, urê là một phương tiện an toàn để cơ thể vận chuyển và bài tiết nitơ dư thừa.
Urê được tổng hợp trong cơ thể của nhiều sinh vật như một phần của chu trình urê , từ quá trình oxy hóa axit amin hoặc từ amoniac . Trong chu trình này, các nhóm amin do amoniac và L- aspartate cung cấp được chuyển thành urê, trong khi L- ornithine , citrulline , L- argininosuccinate , và L- arginine đóng vai trò là chất trung gian. Sản xuất urê xảy ra ở gan và được điều chỉnh bởi N-acetylglutamate . Urê sau đó được hòa tan vào máu (trong phạm vi tham chiếutừ 2,5 đến 6,7 mmol / lít) và được thận vận chuyển và bài tiết ra ngoài như một thành phần của nước tiểu . Ngoài ra, một lượng nhỏ urê được bài tiết (cùng với natri clorua và nước) qua mồ hôi.
Trong nước, các nhóm amin trải qua sự dịch chuyển chậm của các phân tử nước, tạo ra amoniac, ion amoni và ion bicacbonat . Vì lý do này, nước tiểu cũ, ôi thiu có mùi nặng hơn nước tiểu tươi.
Hình ảnh (NH2)2CO trong thực tế
.jpg)
Một số hình ảnh khác về (NH2)2CO
Tổng số đánh giá: 0
Xếp hạng: 5 / 5 sao
Các phương trình điều chế (NH2)2CO
2
NH3
Tên gọi: amoniac
Nguyên tử khối: 17.03052 ± 0.00041
Nhiệt độ sôi: -33°C
Nhiệt độ nóng chảy: -77°C
+
COCl2
Tên gọi: Phosgen
Nguyên tử khối: 129.8392
→
(NH2)2CO
Tên gọi: ure
Nguyên tử khối: 60.0553
Nhiệt độ nóng chảy: 133°C
+
2
HCl
Tên gọi: axit clohidric
Nguyên tử khối: 36.4609
Nhiệt độ sôi: 110°C
Tên gọi: amoniac
Nguyên tử khối: 17.03052 ± 0.00041
Nhiệt độ sôi: -33°C
Nhiệt độ nóng chảy: -77°C
Tên gọi: Phosgen
Nguyên tử khối: 129.8392
Tên gọi: ure
Nguyên tử khối: 60.0553
Nhiệt độ nóng chảy: 133°C
Tên gọi: axit clohidric
Nguyên tử khối: 36.4609
Nhiệt độ sôi: 110°C
Chất xúc tác
không có
Nhiệt độ
Nhiệt độ
Áp suất
thường
Điều kiện khác
không có
3
H2O
Tên gọi: nước
Nguyên tử khối: 18.01528 ± 0.00044
Nhiệt độ sôi: 100°C
Nhiệt độ nóng chảy: 4°C
+
CaCN2
Tên gọi: Canxi cyanamua
Nguyên tử khối: 80.1021
→
(NH2)2CO
Tên gọi: ure
Nguyên tử khối: 60.0553
Nhiệt độ nóng chảy: 133°C
+
Ca(OH)2
Tên gọi: canxi hidroxit hoặc tôi vôi
Nguyên tử khối: 74.0927
Nhiệt độ nóng chảy: 580°C
Tên gọi: nước
Nguyên tử khối: 18.01528 ± 0.00044
Nhiệt độ sôi: 100°C
Nhiệt độ nóng chảy: 4°C
Tên gọi: Canxi cyanamua
Nguyên tử khối: 80.1021
Tên gọi: ure
Nguyên tử khối: 60.0553
Nhiệt độ nóng chảy: 133°C
Tên gọi: canxi hidroxit hoặc tôi vôi
Nguyên tử khối: 74.0927
Nhiệt độ nóng chảy: 580°C
Chất xúc tác
không có
Nhiệt độ
70
Áp suất
thường
Điều kiện khác
không có
2
NH3
Tên gọi: amoniac
Nguyên tử khối: 17.03052 ± 0.00041
Nhiệt độ sôi: -33°C
Nhiệt độ nóng chảy: -77°C
+
CO2
Tên gọi: Cacbon dioxit
Nguyên tử khối: 44.0095
Nhiệt độ sôi: -78°C
Nhiệt độ nóng chảy: -57°C
→
(NH2)2CO
Tên gọi: ure
Nguyên tử khối: 60.0553
Nhiệt độ nóng chảy: 133°C
+
H2O
Tên gọi: nước
Nguyên tử khối: 18.01528 ± 0.00044
Nhiệt độ sôi: 100°C
Nhiệt độ nóng chảy: 4°C
Tên gọi: amoniac
Nguyên tử khối: 17.03052 ± 0.00041
Nhiệt độ sôi: -33°C
Nhiệt độ nóng chảy: -77°C
Tên gọi: Cacbon dioxit
Nguyên tử khối: 44.0095
Nhiệt độ sôi: -78°C
Nhiệt độ nóng chảy: -57°C
Tên gọi: ure
Nguyên tử khối: 60.0553
Nhiệt độ nóng chảy: 133°C
Tên gọi: nước
Nguyên tử khối: 18.01528 ± 0.00044
Nhiệt độ sôi: 100°C
Nhiệt độ nóng chảy: 4°C
Chất xúc tác
không có
Nhiệt độ
180 - 200
Áp suất
200
Điều kiện khác
không có
Các phương trình có (NH2)2CO tham gia phản ứng
(NH2)2CO
Tên gọi: ure
Nguyên tử khối: 60.0553
Nhiệt độ nóng chảy: 133°C
+
H2SO4
Tên gọi: axit sulfuric
Nguyên tử khối: 98.0785
Nhiệt độ sôi: 338°C
Nhiệt độ nóng chảy: 10°C
+
SO3
Tên gọi: sulfuarơ
Nguyên tử khối: 80.0632
Nhiệt độ sôi: 45°C
Nhiệt độ nóng chảy: 16°C
→
CO2
Tên gọi: Cacbon dioxit
Nguyên tử khối: 44.0095
Nhiệt độ sôi: -78°C
Nhiệt độ nóng chảy: -57°C
+
2
NH2SO3H
Tên gọi: Axit sunfamic
Nguyên tử khối: 97.0937
Tên gọi: ure
Nguyên tử khối: 60.0553
Nhiệt độ nóng chảy: 133°C
Tên gọi: axit sulfuric
Nguyên tử khối: 98.0785
Nhiệt độ sôi: 338°C
Nhiệt độ nóng chảy: 10°C
Tên gọi: sulfuarơ
Nguyên tử khối: 80.0632
Nhiệt độ sôi: 45°C
Nhiệt độ nóng chảy: 16°C
Tên gọi: Cacbon dioxit
Nguyên tử khối: 44.0095
Nhiệt độ sôi: -78°C
Nhiệt độ nóng chảy: -57°C
Tên gọi: Axit sunfamic
Nguyên tử khối: 97.0937
Chất xúc tác
không có
Nhiệt độ
thường
Áp suất
thường
Điều kiện khác
không có
(NH2)2CO
Tên gọi: ure
Nguyên tử khối: 60.0553
Nhiệt độ nóng chảy: 133°C
+
H2O
Tên gọi: nước
Nguyên tử khối: 18.01528 ± 0.00044
Nhiệt độ sôi: 100°C
Nhiệt độ nóng chảy: 4°C
+
PbO
Tên gọi: Chì(II) oxit
Nguyên tử khối: 223.1994
Nhiệt độ sôi: 1477°C
Nhiệt độ nóng chảy: 888°C
→
2
NH3
Tên gọi: amoniac
Nguyên tử khối: 17.03052 ± 0.00041
Nhiệt độ sôi: -33°C
Nhiệt độ nóng chảy: -77°C
+
PbCO3
Tên gọi: Chì cacbonat
Nguyên tử khối: 267.2089
Tên gọi: ure
Nguyên tử khối: 60.0553
Nhiệt độ nóng chảy: 133°C
Tên gọi: nước
Nguyên tử khối: 18.01528 ± 0.00044
Nhiệt độ sôi: 100°C
Nhiệt độ nóng chảy: 4°C
Tên gọi: Chì(II) oxit
Nguyên tử khối: 223.1994
Nhiệt độ sôi: 1477°C
Nhiệt độ nóng chảy: 888°C
Tên gọi: amoniac
Nguyên tử khối: 17.03052 ± 0.00041
Nhiệt độ sôi: -33°C
Nhiệt độ nóng chảy: -77°C
Tên gọi: Chì cacbonat
Nguyên tử khối: 267.2089
Chất xúc tác
không có
Nhiệt độ
thường
Áp suất
thường
Điều kiện khác
không có
(NH2)2CO
Tên gọi: ure
Nguyên tử khối: 60.0553
Nhiệt độ nóng chảy: 133°C
→
NH3
Tên gọi: amoniac
Nguyên tử khối: 17.03052 ± 0.00041
Nhiệt độ sôi: -33°C
Nhiệt độ nóng chảy: -77°C
+
HNCO
Tên gọi: Isocyanic acid
Nguyên tử khối: 43.0247
Tên gọi: ure
Nguyên tử khối: 60.0553
Nhiệt độ nóng chảy: 133°C
Tên gọi: amoniac
Nguyên tử khối: 17.03052 ± 0.00041
Nhiệt độ sôi: -33°C
Nhiệt độ nóng chảy: -77°C
Tên gọi: Isocyanic acid
Nguyên tử khối: 43.0247
Chất xúc tác
không có
Nhiệt độ
thường
Áp suất
thường
Điều kiện khác
không có
Một số định nghĩa cơ bản trong hoá học.
Mol là gì?
Trong hóa học, khái niệm mol được dùng để đo lượng chất có chứa 6,022.10²³ số hạt đơn vị nguyên tử hoặc phân tử chất đó. Số 6,02214129×10²³ - được gọi là hằng số Avogadro.
Xem thêmĐộ âm điện là gì?
Độ âm điện là đại lượng đặc trưng định lượng cho khả năng của một nguyên tử trong phân tử hút electron (liên kết) về phía mình.
Xem thêmKim loại là gì?
Kim loại (tiếng Hy Lạp là metallon) là nguyên tố có thể tạo ra các ion dương (cation) và có các liên kết kim loại, và đôi khi người ta cho rằng nó tương tự như là cation trong đám mây các điện tử.
Xem thêmNguyên tử là gì?
Nguyên tử là hạt nhỏ nhất của nguyên tố hóa học không thể chia nhỏ hơn được nữa về mặt hóa học.
Xem thêmPhi kim là gì?
Phi kim là những nguyên tố hóa học dễ nhận electron; ngoại trừ hiđrô, phi kim nằm bên phải bảng tuần hoàn.
Xem thêmNhững sự thật thú vị về hoá học có thể bạn chưa biết.
Interesting facts about hydrogen - the lightest element in the periodic table.
Hydrogen is the first element in the periodic system table. Hydrogen is known to be the lightest of all, the most abundant in the Universe, the essential element for life
Xem thêmInteresting facts about helium
Helium is the first rare gas element in the periodic system table. In the Universe, it ranks second in abundance after elemental hydrogen.
Xem thêmInteresting facts about lithium
Lithium is the alkali metal element, located in the third cell in the periodic table system. Lithium is the lightest of all solid metals and can cut a knife.
Xem thêmInteresting Facts About Beryllium
Beryllium is the lightest alkaline earth metal. Beryllium is found in precious stones such as emeralds and aquamarine. Beryllium and its compounds are both carcinogenic.
Xem thêmInteresting Facts About Carbon
Carbon is the non-metallic element in the sixth cell in the periodic system table. Carbon is one of the most important elements in all life, it is also known as the back.
Xem thêm